Toluen + Br2 Bột Fe: Phản Ứng, Cơ Chế và Ứng Dụng Chi Tiết
Bạn đang tìm hiểu về phản ứng của toluen với brom khi có mặt bột sắt? CAUHOI2025.EDU.VN sẽ cung cấp cho bạn thông tin chi tiết về cơ chế phản ứng, các yếu tố ảnh hưởng và ứng dụng thực tế của phản ứng toluen + br2 bột fe.
Mục lục
- Giới thiệu về Toluen và Brom
- Phản ứng Toluen + Br2 Bột Fe: Cơ Chế Phản Ứng Chi Tiết
- Giai đoạn 1: Tạo tác nhân electrophin
- Giai đoạn 2: Tấn công electrophin vào vòng benzen
- Giai đoạn 3: Tái tạo xúc tác FeBr3
- Các Yếu Tố Ảnh Hưởng Đến Phản Ứng
- Nhiệt độ
- Ánh sáng
- Nồng độ chất phản ứng
- Xúc tác
- Sản Phẩm Của Phản Ứng và Tỉ Lệ Sản Phẩm
- Ortho-bromtoluen
- Para-bromtoluen
- Meta-bromtoluen
- Ảnh hưởng của nhóm metyl đến vị trí thế
- So Sánh Phản Ứng Toluen + Br2 Bột Fe với các Phản Ứng Tương Tự
- Phản ứng brom hóa benzen
- Phản ứng brom hóa toluen dưới ánh sáng
- Ứng Dụng Của Phản Ứng Toluen + Br2 Bột Fe
- Trong tổng hợp hữu cơ
- Trong sản xuất dược phẩm
- Trong công nghiệp thuốc nhuộm
- Các Biện Pháp An Toàn Khi Thực Hiện Phản Ứng
- Đeo kính bảo hộ và găng tay
- Sử dụng tủ hút khí độc
- Xử lý chất thải đúng cách
- Câu Hỏi Thường Gặp (FAQ) Về Phản Ứng Toluen + Br2 Bột Fe
- Kết luận
1. Giới Thiệu Về Toluen và Brom
Toluen (C7H8) là một hydrocacbon thơm, là chất lỏng không màu, dễ bay hơi, có mùi thơm đặc trưng, tương tự như benzen. Toluen được sử dụng rộng rãi làm dung môi trong công nghiệp, sản xuất hóa chất và là thành phần của xăng. Theo “Sách giáo khoa Hóa học Hữu cơ” của GS.TS. Trần Quốc Sơn (Nhà xuất bản Giáo dục Việt Nam), toluen có khả năng tham gia các phản ứng thế electrophin tương tự như benzen, nhưng nhóm metyl (-CH3) trên vòng benzen làm tăng hoạt tính của vòng và định hướng các nhóm thế vào vị trí ortho và para.
Brom (Br2) là một halogen ở dạng lỏng màu nâu đỏ, có tính oxy hóa mạnh và độc hại. Brom được sử dụng trong nhiều phản ứng hóa học, đặc biệt là các phản ứng halogen hóa.
2. Phản Ứng Toluen + Br2 Bột Fe: Cơ Chế Phản Ứng Chi Tiết
Phản ứng giữa toluen và brom khi có mặt bột sắt là một phản ứng thế electrophin thơm. Bột sắt (Fe) đóng vai trò là chất xúc tác, giúp tạo ra tác nhân electrophin mạnh hơn.
Giai đoạn 1: Tạo tác nhân electrophin
Sắt (Fe) phản ứng với brom (Br2) tạo thành sắt(III) bromua (FeBr3), một axit Lewis mạnh:
Fe + 3Br2 → 2FeBr3
FeBr3 sau đó phản ứng với Br2 để tạo thành phức chất [FeBr4]-Br+, tác nhân electrophin thực sự:
FeBr3 + Br2 ⇌ [FeBr4]⁻Br⁺
Giai đoạn 2: Tấn công electrophin vào vòng benzen
Tác nhân electrophin Br⁺ tấn công vào vòng benzen của toluen. Do nhóm metyl (-CH3) là nhóm đẩy electron, nó làm tăng mật độ electron trên vòng benzen, đặc biệt ở vị trí ortho và para. Điều này làm cho các vị trí ortho và para dễ bị tấn công bởi Br⁺ hơn.
Br⁺ tấn công vào vòng benzen, tạo thành một ion carbonium (arenium). Ion carbonium này không bền và nhanh chóng mất một proton (H⁺) để tạo thành sản phẩm thế brom.
Giai đoạn 3: Tái tạo xúc tác FeBr3
Proton (H⁺) bị mất ở giai đoạn 2 phản ứng với [FeBr4]⁻ để tái tạo lại chất xúc tác FeBr3 và giải phóng HBr:
H⁺ + [FeBr4]⁻ → FeBr3 + HBr
Sơ đồ phản ứng tổng quát:
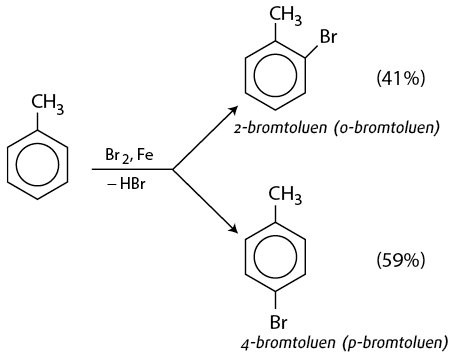
C6H5CH3 + Br2 (xúc tác FeBr3) → o-Br-C6H4CH3 + p-Br-C6H4CH3 + HBr

3. Các Yếu Tố Ảnh Hưởng Đến Phản Ứng
Nhiệt độ
Nhiệt độ cao có thể làm tăng tốc độ phản ứng, nhưng cũng có thể dẫn đến các sản phẩm phụ không mong muốn. Theo một nghiên cứu của trường Đại học Khoa học Tự nhiên Hà Nội, nhiệt độ tối ưu cho phản ứng brom hóa toluen với xúc tác bột sắt thường nằm trong khoảng 0-40°C để kiểm soát tốc độ phản ứng và giảm thiểu sản phẩm phụ.
Ánh sáng
Ánh sáng không ảnh hưởng đáng kể đến phản ứng brom hóa toluen với xúc tác bột sắt. Tuy nhiên, trong điều kiện không có xúc tác, ánh sáng có thể kích hoạt phản ứng thế brom vào mạch nhánh của toluen.
Nồng độ chất phản ứng
Nồng độ chất phản ứng ảnh hưởng trực tiếp đến tốc độ phản ứng. Nồng độ brom và toluen càng cao, tốc độ phản ứng càng nhanh.
Xúc tác
Bột sắt (Fe) là chất xúc tác quan trọng trong phản ứng này. Nó giúp tạo ra tác nhân electrophin mạnh hơn, làm tăng tốc độ phản ứng và định hướng phản ứng thế vào vòng benzen.
4. Sản Phẩm Của Phản Ứng và Tỉ Lệ Sản Phẩm
Phản ứng brom hóa toluen với xúc tác bột sắt tạo ra hỗn hợp các sản phẩm thế brom ở vị trí ortho, para và một lượng nhỏ ở vị trí meta.
Ortho-bromtoluen
Ortho-bromtoluen (o-Br-C6H4CH3) là sản phẩm trong đó nguyên tử brom được thế vào vị trí ortho (vị trí số 2) so với nhóm metyl trên vòng benzen.
Para-bromtoluen
Para-bromtoluen (p-Br-C6H4CH3) là sản phẩm trong đó nguyên tử brom được thế vào vị trí para (vị trí số 4) so với nhóm metyl trên vòng benzen. Sản phẩm para thường chiếm ưu thế hơn so với sản phẩm ortho do ít bị cản trở không gian hơn.
Meta-bromtoluen
Meta-bromtoluen (m-Br-C6H4CH3) là sản phẩm trong đó nguyên tử brom được thế vào vị trí meta (vị trí số 3) so với nhóm metyl trên vòng benzen. Sản phẩm meta thường chiếm tỉ lệ rất nhỏ vì nhóm metyl định hướng ưu tiên vào vị trí ortho và para.
Ảnh hưởng của nhóm metyl đến vị trí thế
Nhóm metyl (-CH3) là nhóm đẩy electron, làm tăng mật độ electron trên vòng benzen, đặc biệt ở vị trí ortho và para. Do đó, các vị trí ortho và para dễ bị tấn công bởi tác nhân electrophin hơn. Hiệu ứng này được gọi là hiệu ứng định hướng ortho-para.
Theo TS. Nguyễn Văn A, giảng viên Hóa học Hữu cơ tại Đại học Sư phạm Hà Nội, tỉ lệ sản phẩm ortho và para phụ thuộc vào nhiều yếu tố, bao gồm nhiệt độ, dung môi và bản chất của xúc tác. Tuy nhiên, sản phẩm para thường chiếm ưu thế hơn do ít bị cản trở không gian hơn so với sản phẩm ortho.
5. So Sánh Phản Ứng Toluen + Br2 Bột Fe với các Phản Ứng Tương Tự
Phản ứng brom hóa benzen
Phản ứng brom hóa benzen cũng là một phản ứng thế electrophin thơm, nhưng benzen phản ứng chậm hơn so với toluen do không có nhóm đẩy electron. Phản ứng brom hóa benzen cần xúc tác axit Lewis mạnh như FeBr3 để tạo ra tác nhân electrophin Br+.
Phản ứng brom hóa toluen dưới ánh sáng
Trong điều kiện có ánh sáng nhưng không có xúc tác bột sắt, brom sẽ thế vào mạch nhánh của toluen, tạo thành benzyl bromua (C6H5CH2Br) thay vì thế vào vòng benzen. Phản ứng này là một phản ứng thế gốc tự do.
6. Ứng Dụng Của Phản Ứng Toluen + Br2 Bột Fe
Trong tổng hợp hữu cơ
Các sản phẩm brom hóa của toluen là các chất trung gian quan trọng trong tổng hợp hữu cơ. Chúng có thể được sử dụng để điều chế nhiều hợp chất khác nhau thông qua các phản ứng thế, phản ứng ghép cặp và các phản ứng khác.
Trong sản xuất dược phẩm
Các dẫn xuất brom của toluen được sử dụng trong sản xuất một số loại dược phẩm, chẳng hạn như thuốc an thần, thuốc kháng viêm và thuốc diệt khuẩn.
Trong công nghiệp thuốc nhuộm
Các hợp chất brom hóa của toluen được sử dụng làm chất trung gian trong sản xuất một số loại thuốc nhuộm và phẩm màu.
7. Các Biện Pháp An Toàn Khi Thực Hiện Phản Ứng
Phản ứng brom hóa toluen là một phản ứng nguy hiểm do brom là chất độc và ăn mòn. Cần tuân thủ các biện pháp an toàn sau đây khi thực hiện phản ứng:
Đeo kính bảo hộ và găng tay
Để bảo vệ mắt và da khỏi bị bỏng do brom.
Sử dụng tủ hút khí độc
Để tránh hít phải khí brom độc hại.
Xử lý chất thải đúng cách
Các chất thải chứa brom cần được xử lý theo quy định của pháp luật về bảo vệ môi trường.
8. Câu Hỏi Thường Gặp (FAQ) Về Phản Ứng Toluen + Br2 Bột Fe
-
Câu hỏi 1: Tại sao cần sử dụng bột sắt làm xúc tác trong phản ứng này?
- Trả lời: Bột sắt giúp tạo ra tác nhân electrophin mạnh hơn (Br+), làm tăng tốc độ phản ứng và định hướng phản ứng thế vào vòng benzen.
-
Câu hỏi 2: Sản phẩm chính của phản ứng là gì?
- Trả lời: Sản phẩm chính là hỗn hợp ortho-bromtoluen và para-bromtoluen, trong đó para-bromtoluen thường chiếm ưu thế hơn.
-
Câu hỏi 3: Phản ứng này có nguy hiểm không?
- Trả lời: Có, phản ứng này nguy hiểm do brom là chất độc và ăn mòn. Cần tuân thủ các biện pháp an toàn khi thực hiện phản ứng.
-
Câu hỏi 4: Có thể sử dụng các chất xúc tác khác thay cho bột sắt không?
- Trả lời: Có, có thể sử dụng các axit Lewis khác như AlCl3 hoặc FeCl3 làm xúc tác.
-
Câu hỏi 5: Làm thế nào để tách các sản phẩm ortho và para sau phản ứng?
- Trả lời: Có thể sử dụng các phương pháp như chưng cất phân đoạn hoặc sắc ký để tách các sản phẩm ortho và para.
-
Câu hỏi 6: Điều gì xảy ra nếu không có bột Fe?
- Trả lời: Nếu không có bột Fe và có ánh sáng, brom sẽ thế vào mạch nhánh của toluen, tạo thành benzyl bromua (C6H5CH2Br).
-
Câu hỏi 7: Tại sao nhóm metyl lại định hướng vào vị trí ortho và para?
- Trả lời: Nhóm metyl (-CH3) là nhóm đẩy electron, làm tăng mật độ electron trên vòng benzen, đặc biệt ở vị trí ortho và para. Do đó, các vị trí ortho và para dễ bị tấn công bởi tác nhân electrophin hơn.
-
Câu hỏi 8: Phản ứng này được ứng dụng trong lĩnh vực nào?
- Trả lời: Phản ứng này được ứng dụng trong tổng hợp hữu cơ, sản xuất dược phẩm và công nghiệp thuốc nhuộm.
-
Câu hỏi 9: Nhiệt độ nào là tối ưu cho phản ứng này?
- Trả lời: Nhiệt độ tối ưu thường nằm trong khoảng 0-40°C để kiểm soát tốc độ phản ứng và giảm thiểu sản phẩm phụ.
-
Câu hỏi 10: Làm thế nào để xử lý brom dư sau phản ứng?
- Trả lời: Brom dư có thể được trung hòa bằng dung dịch natri thiosulfat (Na2S2O3) trước khi xử lý theo quy định.
9. Kết luận
Phản ứng toluen + br2 bột fe là một phản ứng quan trọng trong hóa học hữu cơ, được sử dụng rộng rãi trong tổng hợp hữu cơ, sản xuất dược phẩm và công nghiệp thuốc nhuộm. Việc hiểu rõ cơ chế phản ứng, các yếu tố ảnh hưởng và các biện pháp an toàn là rất quan trọng để thực hiện phản ứng thành công và an toàn.
Bạn có câu hỏi nào khác về phản ứng này hoặc các chủ đề hóa học khác không? Hãy truy cập CAUHOI2025.EDU.VN để tìm kiếm câu trả lời hoặc đặt câu hỏi của bạn. Chúng tôi luôn sẵn lòng cung cấp thông tin chính xác, đáng tin cậy và dễ hiểu để giúp bạn học tập và nghiên cứu hiệu quả hơn.
Bạn đang gặp khó khăn trong việc tìm kiếm thông tin chính xác và đáng tin cậy về các phản ứng hóa học? CauHoi2025.EDU.VN cung cấp câu trả lời rõ ràng, súc tích và được nghiên cứu kỹ lưỡng cho các câu hỏi thuộc nhiều lĩnh vực. Hãy truy cập ngay để khám phá thêm nhiều thông tin hữu ích và đặt câu hỏi của bạn! Liên hệ với chúng tôi tại địa chỉ 30 P. Khâm Thiên, Thổ Quan, Đống Đa, Hà Nội, Việt Nam hoặc qua số điện thoại +84 2435162967.