**Nitơ Hóa Trị Mấy? Tính Chất và Ứng Dụng Chi Tiết Của Nitơ**
Bạn đang thắc mắc nitơ hóa trị mấy? Nitơ là một nguyên tố hóa học vô cùng quan trọng đối với sự sống trên Trái Đất và cơ thể con người. Bài viết này của CAUHOI2025.EDU.VN sẽ cung cấp thông tin chi tiết về hóa trị của nitơ, tính chất đặc trưng và các ứng dụng thực tiễn của nó trong đời sống và công nghiệp. Khám phá ngay để hiểu rõ hơn về nguyên tố này!
Nitơ (N2) là một thành phần thiết yếu của khí quyển và đóng vai trò then chốt trong nhiều quá trình sinh học. Nó có mặt trong các hợp chất quan trọng như protein và axit nucleic, những “viên gạch” xây dựng nên sự sống. Hiểu rõ về nitơ giúp chúng ta ứng dụng hiệu quả nguyên tố này vào nhiều lĩnh vực khác nhau.
1. Nitơ Là Gì?
Nitơ, ký hiệu hóa học là N2, là một nguyên tố chiếm phần lớn khí quyển Trái Đất và đóng vai trò quan trọng đối với sự sống. Nó tham gia vào quá trình bảo vệ hành tinh khỏi bức xạ mặt trời.
Nitơ tồn tại ở hai dạng chính: nitơ lỏng và nitơ khí. Nitơ lỏng có nhiều đặc tính hữu ích và được ứng dụng rộng rãi trong nhiều lĩnh vực. Trong tự nhiên, nitơ tồn tại ở dạng tự do và hợp chất, là thành phần của nhiều hợp chất hữu cơ như axit nucleic và protein.

2. Nitơ Hóa Trị Mấy?
Không giống như nhiều chất khí khác chỉ có một hóa trị duy nhất, nitơ có thể thể hiện nhiều hóa trị khác nhau, bao gồm hóa trị II, III và IV. Sự đa dạng này cho phép nitơ tham gia vào nhiều loại hợp chất và phản ứng hóa học.
3. Số Oxi Hóa Của Nitơ Là Gì?
Nitơ có nhiều số oxi hóa khác nhau, bao gồm -3, 0, +1, +2, +3, +4 và +5. Điều này cho phép nitơ vừa có tính khử, vừa có tính oxi hóa, tùy thuộc vào điều kiện phản ứng.
4. Tính Chất Của Nitơ
4.1. Tính Chất Vật Lý
Nitơ là chất khí nhẹ hơn không khí, không màu, không mùi, không vị và ít tan trong nước. Nó hóa rắn ở nhiệt độ rất thấp, khoảng -196°C.
Một số thông tin khác về nitơ:
- Ký hiệu nguyên tử: N
- Số hiệu nguyên tử: 7, thuộc nhóm VA
- Số oxi hóa: -3, 0, +1, +2, +3, +4, +5
- Nhiệt độ sôi: 77,36K
- Nhiệt độ nóng chảy: 63,15K

4.2. Tính Chất Hóa Học
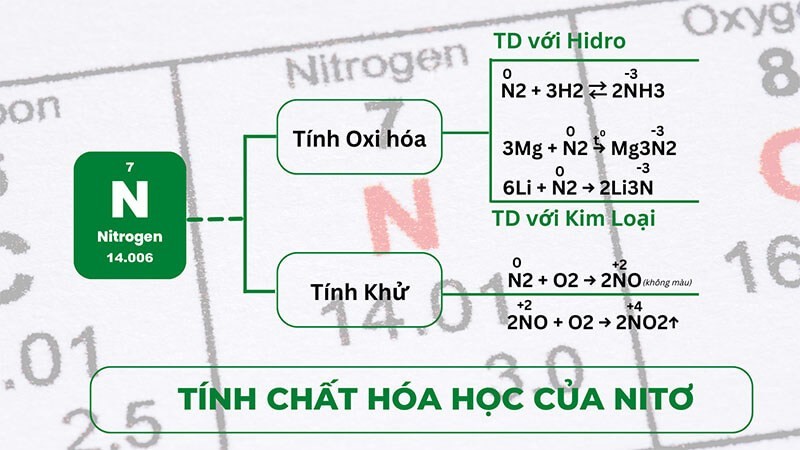
Nitơ có nhiều số oxi hóa khác nhau, do đó nó vừa có tính khử, vừa có tính oxi hóa. Tuy nhiên, nitơ trơ về mặt hóa học ở nhiệt độ thường và hoạt động mạnh hơn ở nhiệt độ cao.
Tính khử của nitơ:
-
Nitơ phản ứng với các nguyên tố có độ âm điện lớn hơn, đặc biệt ở nhiệt độ cao (trên 3000°C), tạo thành nitơ monoxit (NO).
Phương trình phản ứng: N2 + O2 → 2NO (không màu)
Trong đó, N2 có hóa trị 0, N trong NO có hóa trị +2.
-
Ở điều kiện thường, nitơ monoxit tác dụng với oxi trong không khí tạo thành nitơ đioxit (NO2) có màu nâu đỏ.
Phương trình phản ứng: 2NO + O2 → 2NO2
Trong đó, N trong NO2 có hóa trị +4.
Tính oxi hóa của nitơ:
Nitơ tác dụng với các nguyên tố có độ âm điện nhỏ hơn, bao gồm kim loại và hidro:
-
Tác dụng với kim loại:
-
Ở điều kiện thường, nitơ chỉ tác dụng với liti (Li) tạo thành liti nitrua.
Phương trình: 6Li + N2 → 2Li3N
-
Ở nhiệt độ cao, nitơ tác dụng với nhiều kim loại khác tạo thành nitrua. Nitrua dễ bị thủy phân tạo thành NH3.
Phương trình: 3Mg + N2 → Mg3N2
-
-
Tác dụng với hidro:
Nitơ phản ứng với hidro ở nhiệt độ và áp suất cao, có chất xúc tác, tạo thành amoniac.
Phương trình phản ứng: N2 + 3H2 ⇄ 2NH3
Theo “Sách giáo khoa Hóa học lớp 10” của Nhà xuất bản Giáo dục Việt Nam, nitơ có cấu hình electron đặc biệt với liên kết ba rất bền, do đó nó tương đối trơ ở điều kiện thường. Tuy nhiên, ở nhiệt độ cao hoặc có xúc tác, nó có thể tham gia vào nhiều phản ứng hóa học quan trọng.
5. Ứng Dụng Của Nitơ
Nhờ các tính chất đặc biệt, nitơ được ứng dụng rộng rãi trong nhiều lĩnh vực:
- Trong nghiên cứu và giáo dục: Phân tích mẫu và nghiên cứu các hợp chất hóa học.
- Trong chế biến và vận chuyển thực phẩm: Làm lạnh để bảo quản thực phẩm an toàn.
- Trong y học: Bảo quản các bộ phận cơ thể, đặc biệt là trứng và tinh trùng.
- Trong chế tác kim loại và luyện kim: Sản xuất thép không gỉ, linh kiện điện tử…
- Trong sản xuất máy bay và lốp ô tô: Bơm lốp ô tô và máy bay.
- Trong chế biến kim loại và hàn ống: Làm sạch đường ống, hạn chế hư hại.
- Trong bảo quản thực phẩm: Ngăn chặn quá trình oxi hóa, giúp thực phẩm tươi lâu hơn.
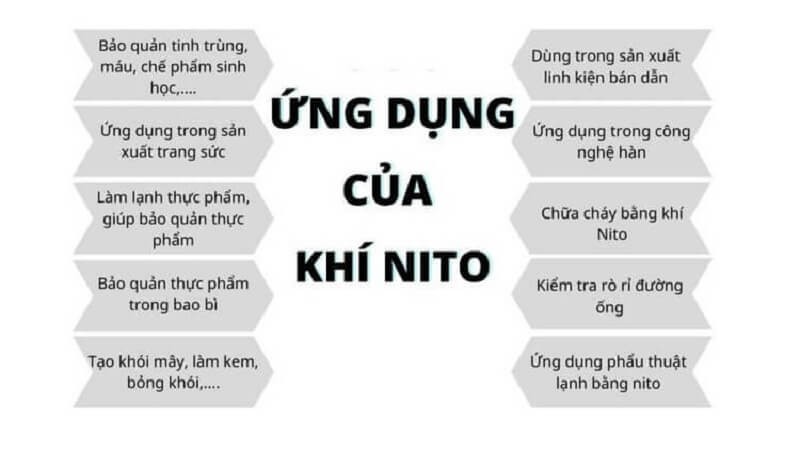
Theo thống kê của Tổng cục Thống kê Việt Nam năm 2023, ngành công nghiệp thực phẩm và đồ uống là một trong những ngành sử dụng nitơ nhiều nhất, đặc biệt trong quy trình đóng gói và bảo quản sản phẩm.
6. Điều Chế Nitơ
Trong phòng thí nghiệm:
Sử dụng dung dịch muối amoni nitrit bão hòa là phương pháp phổ biến để điều chế nitơ trong phòng thí nghiệm.
Trong công nghiệp:
Nitơ được điều chế bằng cách chưng cất phân đoạn không khí lỏng. Nitơ thu được ở nhiệt độ -196°C và lưu trữ trong bình thép nén với áp suất 125atm.
7. Các Câu Hỏi Thường Gặp Về Nitơ (FAQ)
7.1. Tại sao nitơ lại quan trọng đối với sự sống?
Nitơ là thành phần cấu tạo của protein và axit nucleic, hai hợp chất thiết yếu cho mọi sinh vật sống.
7.2. Nitơ lỏng có nguy hiểm không?
Nitơ lỏng rất lạnh và có thể gây bỏng lạnh nếu tiếp xúc trực tiếp với da.
7.3. Làm thế nào để bảo quản thực phẩm bằng nitơ?
Nitơ được sử dụng để loại bỏ oxy trong bao bì thực phẩm, ngăn chặn quá trình oxi hóa và kéo dài thời gian bảo quản.
7.4. Nitơ có tác động tiêu cực đến môi trường không?
Việc sử dụng quá nhiều phân bón chứa nitơ có thể gây ô nhiễm nguồn nước và không khí.
7.5. Ứng dụng nào của nitơ là quan trọng nhất?
Ứng dụng quan trọng nhất của nitơ có lẽ là trong sản xuất phân bón, giúp tăng năng suất cây trồng và đảm bảo an ninh lương thực.
7.6. Nitơ có thể tái chế được không?
Nitơ trong khí quyển là một nguồn tài nguyên vô tận và có thể được tái sử dụng thông qua các quy trình công nghiệp.
7.7. Sự khác biệt giữa nitơ và các khí trơ khác là gì?
Nitơ không phải là khí trơ hoàn toàn. Nó có thể phản ứng với các chất khác ở điều kiện thích hợp, trong khi các khí trơ khác rất khó phản ứng.
7.8. Nitơ có ảnh hưởng đến sức khỏe con người không?
Nitơ là một phần của không khí chúng ta hít thở và không gây hại ở nồng độ bình thường. Tuy nhiên, nitơ có thể gây ngạt nếu nồng độ oxy trong không khí quá thấp.
7.9. Nitơ được sử dụng trong ngành công nghiệp điện tử như thế nào?
Nitơ được sử dụng để tạo môi trường trơ trong quá trình sản xuất linh kiện điện tử, ngăn chặn quá trình oxy hóa và đảm bảo chất lượng sản phẩm.
7.10. Nitơ có vai trò gì trong ngành hàng không?
Nitơ được sử dụng để bơm lốp máy bay, giúp giảm nguy cơ cháy nổ và đảm bảo an toàn khi hạ cánh.
Nitơ hóa trị mấy, tính chất và ứng dụng của nó đã được trình bày chi tiết trong bài viết này. Hy vọng những thông tin này sẽ giúp bạn giải đáp mọi thắc mắc. Nếu bạn cần tìm hiểu thêm thông tin hoặc có bất kỳ câu hỏi nào, đừng ngần ngại truy cập CAUHOI2025.EDU.VN để được hỗ trợ.
Bạn đang gặp khó khăn trong việc tìm kiếm thông tin hóa học chính xác và đáng tin cậy? Bạn cảm thấy choáng ngợp trước vô vàn nguồn tin trên mạng? Hãy đến với CAUHOI2025.EDU.VN, nơi bạn có thể tìm thấy câu trả lời cho mọi thắc mắc về hóa học, từ những khái niệm cơ bản đến các vấn đề phức tạp.
Liên hệ với CAUHOI2025.EDU.VN:
Địa chỉ: 30 P. Khâm Thiên, Thổ Quan, Đống Đa, Hà Nội, Việt Nam
Số điện thoại: +84 2435162967
Trang web: CauHoi2025.EDU.VN
Tôm Sú – Hướng Dẫn Toàn Diện Từ Chọn Mua Đến Nuôi Trồng | VIETCHEM
Khám phá tất cả về tôm sú: đặc điểm, giá trị dinh dưỡng, giá 1kg, cách chọn tôm tươi & bí quyết nuôi trồng bền vững từ chuyên gia 20 năm kinh nghiệm VIETCHEM.
0
Sodium Hydroxide (NaOH): Định Nghĩa, Tính Chất, Ứng Dụng
Tìm hiểu Sodium Hydroxide là gì (NaOH, xút ăn da), tính chất, ứng dụng đa ngành (công nghiệp, xà phòng, mỹ phẩm). Hướng dẫn an toàn và địa chỉ mua uy tín.
0
Đồng Đen Là Gì? Sự Thật Khoa Học , Lời Đồn & Giá Trị Thực
Đồng đen được xem là một loại kim loại biến thể của Đồng (Cu) nhưng lại cực kỳ quý hiếm, bí ẩn và linh thiêng. Trong văn hóa dân gian Việt Nam nói riêng và các quốc gia Châu Á nói chung.
0
FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4+ H2OTừ Phương Trình Đến Ứng Dụng Thực Tiễn
Phương trình FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4+ H2O – VIETCHEM sẽ giúp bạn hiểu chi tiết phản ứng FeSO4 tác dụng với KMnO4 trong môi trường H2SO4