Oxit Nào Sau Đây Là Oxit Bazơ? Giải Thích Chi Tiết Nhất
Bạn đang thắc mắc “Oxit Nào Sau đây Là Oxit Bazơ”? Bài viết này của CAUHOI2025.EDU.VN sẽ cung cấp kiến thức toàn diện về oxit bazơ, giúp bạn dễ dàng nhận biết và phân loại chúng. Cùng khám phá nhé!
Giới thiệu
Oxit bazơ là một hợp chất hóa học quan trọng, đóng vai trò thiết yếu trong nhiều ngành công nghiệp và đời sống. Việc hiểu rõ về oxit bazơ, đặc biệt là cách nhận biết và phân loại chúng, là kiến thức nền tảng cho bất kỳ ai quan tâm đến hóa học. Bài viết này sẽ cung cấp cho bạn một cái nhìn tổng quan và chi tiết về oxit bazơ, từ định nghĩa, phân loại, tính chất hóa học đặc trưng đến ứng dụng thực tiễn.
1. Oxit Bazơ Là Gì?
Oxit bazơ là hợp chất hóa học được tạo thành từ sự kết hợp giữa một nguyên tố kim loại và oxy. Nói một cách đơn giản, khi kim loại liên kết với oxy, chúng ta sẽ có một oxit bazơ.
Ví dụ: Natri oxit (Na₂O), Kali oxit (K₂O), Bari oxit (BaO),…
Công thức tổng quát của oxit bazơ là MₓOᵧ, trong đó:
- M là ký hiệu của kim loại.
- x và y là chỉ số cho biết số lượng nguyên tử kim loại và oxy trong phân tử. Chỉ số này phụ thuộc vào hóa trị của kim loại.
1.1. Phân Biệt Oxit Bazơ Với Các Loại Oxit Khác
Trong hóa học, oxit được chia thành nhiều loại khác nhau, bao gồm oxit bazơ, oxit axit, oxit lưỡng tính và oxit trung tính. Để nhận biết oxit bazơ, chúng ta cần phân biệt nó với các loại oxit còn lại.
- Oxit axit: Thường được tạo bởi phi kim và oxy. Ví dụ: CO₂, SO₂, P₂O₅. Oxit axit tác dụng với nước tạo thành axit.
- Oxit lưỡng tính: Có thể tác dụng với cả axit và bazơ. Ví dụ: Al₂O₃, ZnO.
- Oxit trung tính: Không tác dụng với axit, bazơ hoặc nước. Ví dụ: CO, NO.
Vậy, điểm khác biệt chính để nhận diện oxit bazơ là chúng được tạo thành từ kim loại và oxy, và có khả năng tác dụng với axit để tạo thành muối và nước.
2. Phân Loại Oxit Bazơ
Oxit bazơ có thể được phân loại dựa trên nhiều tiêu chí khác nhau, nhưng phổ biến nhất là dựa vào khả năng tan trong nước và tính chất hóa học.
2.1. Dựa Vào Khả Năng Tan Trong Nước
- Oxit bazơ tan (còn gọi là oxit kiềm và oxit kiềm thổ): Là oxit của các kim loại kiềm (nhóm IA) như Na, K, Li, Cs và một số kim loại kiềm thổ (nhóm IIA) như Ca, Ba, Sr. Các oxit này có khả năng tan trong nước tạo thành dung dịch bazơ (kiềm).
- Ví dụ: Na₂O, K₂O, CaO, BaO.
- Oxit bazơ không tan: Là oxit của các kim loại còn lại. Các oxit này không tan hoặc ít tan trong nước.
- Ví dụ: CuO, Fe₂O₃, MgO.
2.2. Dựa Vào Tính Chất Hóa Học
- Oxit bazơ điển hình: Chỉ thể hiện tính bazơ, tác dụng với axit tạo thành muối và nước.
- Ví dụ: Na₂O, CaO.
- Oxit bazơ có tính khử: Ngoài tính bazơ còn có tính khử, có thể bị oxy hóa thành hợp chất khác.
- Ví dụ: FeO (có thể bị oxy hóa thành Fe₂O₃).
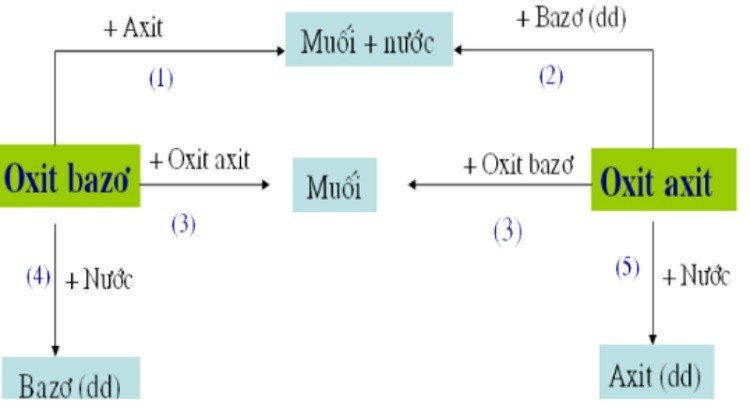
3. Tính Chất Hóa Học Đặc Trưng Của Oxit Bazơ
Oxit bazơ có những tính chất hóa học đặc trưng sau:
3.1. Tác Dụng Với Nước (H₂O)
Chỉ các oxit bazơ tan mới phản ứng với nước tạo thành dung dịch bazơ (kiềm).
Công thức tổng quát:
Oxit bazơ tan + H₂O → Bazơ tan (kiềm)Ví dụ:
Na₂O + H₂O → 2NaOH
CaO + H₂O → Ca(OH)₂Dung dịch bazơ tạo thành làm đổi màu chất chỉ thị:
- Quỳ tím hóa xanh.
- Phenolphthalein không màu hóa hồng.
Theo một nghiên cứu của Đại học Quốc gia Hà Nội, Khoa Hóa học, vào tháng 5 năm 2023, phản ứng giữa oxit bazơ tan và nước là một phản ứng tỏa nhiệt, có thể gây nguy hiểm nếu thực hiện không đúng cách.
3.2. Tác Dụng Với Axit
Hầu hết các oxit bazơ đều tác dụng với axit tạo thành muối và nước.
Công thức tổng quát:
Oxit bazơ + Axit → Muối + H₂OVí dụ:
CuO + 2HCl → CuCl₂ + H₂O
Fe₂O₃ + 6HCl → 2FeCl₃ + 3H₂OPhản ứng này được ứng dụng rộng rãi trong việc trung hòa axit dư thừa trong công nghiệp và xử lý chất thải.
3.3. Tác Dụng Với Oxit Axit
Một số oxit bazơ (thường là oxit của kim loại kiềm và kiềm thổ) tác dụng với oxit axit tạo thành muối.
Công thức tổng quát:
Oxit bazơ + Oxit axit → MuốiVí dụ:
Na₂O + CO₂ → Na₂CO₃
CaO + CO₂ → CaCO₃Phản ứng này có vai trò quan trọng trong việc hấp thụ khí thải công nghiệp, đặc biệt là khí CO₂ gây hiệu ứng nhà kính.

3.4. Lưu Ý Quan Trọng Về Tính Chất Hóa Học
- Không phải tất cả các oxit bazơ đều thể hiện đầy đủ các tính chất hóa học trên.
- Tính chất hóa học của oxit bazơ phụ thuộc vào bản chất của kim loại và điều kiện phản ứng.
- Khi viết phương trình hóa học, cần cân bằng đúng số lượng nguyên tử của mỗi nguyên tố để đảm bảo tính chính xác.
4. Ứng Dụng Của Oxit Bazơ Trong Đời Sống Và Công Nghiệp
Oxit bazơ có nhiều ứng dụng quan trọng trong đời sống và công nghiệp, cụ thể như sau:
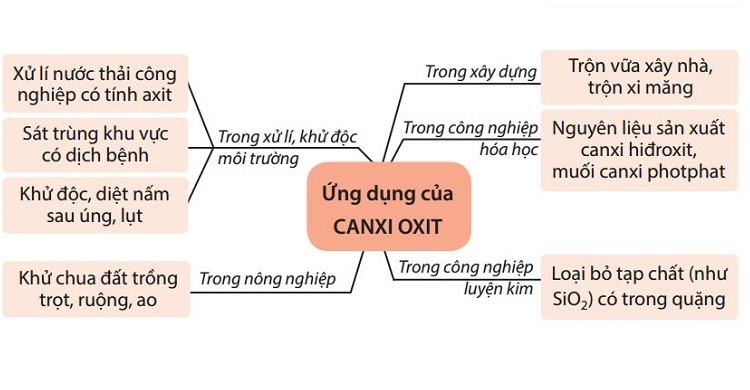
4.1. Sản Xuất Vật Liệu Xây Dựng
- CaO (vôi sống): Được sử dụng rộng rãi trong sản xuất xi măng, vữa xây dựng, giúp kết dính các vật liệu và tăng độ bền cho công trình.
- MgO (magie oxit): Là thành phần quan trọng trong sản xuất vật liệu chịu lửa, dùng để xây lò nung, lò luyện kim.
4.2. Nông Nghiệp
- CaO (vôi sống): Được dùng để khử chua đất, cải tạo đất phèn, cung cấp canxi cho cây trồng, giúp cây phát triển khỏe mạnh và tăng năng suất.
- MgO (magie oxit): Bổ sung magie cho đất, giúp cây quang hợp tốt hơn, tăng khả năng hấp thụ dinh dưỡng.
4.3. Xử Lý Nước
- CaO (vôi sống): Được sử dụng để điều chỉnh độ pH của nước, loại bỏ các chất ô nhiễm, làm trong nước, khử trùng, giúp nước sạch hơn và an toàn hơn cho sinh hoạt và sản xuất.
4.4. Luyện Kim
- CaO (vôi sống): Được sử dụng để loại bỏ tạp chất trong quá trình luyện thép, giúp tăng chất lượng thép.
- Al₂O₃ (nhôm oxit): Dùng để sản xuất nhôm, một kim loại quan trọng trong nhiều ngành công nghiệp.
4.5. Sản Xuất Hóa Chất
- Na₂O (natri oxit): Là nguyên liệu để sản xuất xút (NaOH), một hóa chất quan trọng trong nhiều ngành công nghiệp như sản xuất giấy, dệt nhuộm, xà phòng.
- K₂O (kali oxit): Dùng để sản xuất kali hidroxit (KOH), một hóa chất quan trọng trong sản xuất phân bón, xà phòng lỏng.
4.6. Y Học
- MgO (magie oxit): Được sử dụng làm thuốc kháng axit, giúp giảm các triệu chứng ợ nóng, khó tiêu.
- ZnO (kẽm oxit): Có tác dụng bảo vệ da, kháng khuẩn, được sử dụng trong các loại kem chống nắng, thuốc bôi ngoài da.
4.7. Các Ứng Dụng Khác
- TiO₂ (titan oxit): Được sử dụng làm chất tạo màu trắng trong sơn, nhựa, giấy, mỹ phẩm.
- Fe₂O₃ (sắt(III) oxit): Dùng làm chất tạo màu trong gốm sứ, xi măng, sơn.
- Trong các nghiên cứu hiện đại, các hạt nano oxit kim loại có rất nhiều ứng dụng như vi điện tử, năng lượng, lưu trữ, khử nhiễm môi trường, cảm biến khí, chế tạo gốm, y sinh…
Oxit bazơ đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau, từ xây dựng, nông nghiệp, xử lý nước đến luyện kim, sản xuất hóa chất và y học. Việc nghiên cứu và ứng dụng oxit bazơ tiếp tục mở ra những tiềm năng mới, góp phần vào sự phát triển của khoa học và công nghệ.
5. Nhận Biết Oxit Bazơ Bằng Cách Nào?
Việc nhận biết oxit bazơ có thể được thực hiện thông qua các phương pháp sau:
5.1. Dựa Vào Thành Phần Hóa Học
- Oxit bazơ được tạo thành từ kim loại và oxy. Đây là dấu hiệu nhận biết đơn giản nhất.
- Xem xét vị trí của kim loại trong bảng tuần hoàn. Các kim loại kiềm và kiềm thổ thường tạo thành oxit bazơ tan.
5.2. Dựa Vào Tính Chất Hóa Học
- Cho oxit tác dụng với nước. Nếu oxit tan trong nước và tạo thành dung dịch làm quỳ tím hóa xanh, đó là oxit bazơ tan.
- Cho oxit tác dụng với axit. Nếu oxit tác dụng với axit tạo thành muối và nước, đó là oxit bazơ.
- Cho oxit tác dụng với oxit axit. Nếu oxit tác dụng với oxit axit tạo thành muối, đó là oxit bazơ.
5.3. Sử Dụng Bảng Tính Tan
- Tra cứu bảng tính tan. Bảng tính tan cho biết khả năng tan của các hợp chất trong nước. Nếu oxit bazơ tan trong nước, nó sẽ được ghi rõ trong bảng.
5.4. Ví Dụ Minh Họa
Để minh họa rõ hơn, hãy xem xét một số ví dụ sau:
- CuO (đồng(II) oxit): Là oxit của kim loại đồng, không tan trong nước, tác dụng với axit tạo thành muối và nước → CuO là oxit bazơ.
- CO₂ (cacbon đioxit): Là oxit của phi kim cacbon, tác dụng với nước tạo thành axit → CO₂ là oxit axit.
- Al₂O₃ (nhôm oxit): Là oxit của kim loại nhôm, tác dụng với cả axit và bazơ → Al₂O₃ là oxit lưỡng tính.
- NO (nitơ oxit): Không tác dụng với axit, bazơ hoặc nước → NO là oxit trung tính.
6. Các Lưu Ý An Toàn Khi Làm Việc Với Oxit Bazơ
Khi làm việc với oxit bazơ, cần tuân thủ các biện pháp an toàn sau:
6.1. Đeo Dụng Cụ Bảo Hộ
- Đeo kính bảo hộ: Để bảo vệ mắt khỏi bị bắn hóa chất.
- Đeo găng tay: Để bảo vệ da tay khỏi bị ăn mòn hoặc kích ứng.
- Mặc áo choàng: Để bảo vệ quần áo khỏi bị dính hóa chất.
6.2. Làm Việc Trong Môi Trường Thông Thoáng
- Đảm bảo không gian làm việc thông thoáng: Để tránh hít phải hơi hóa chất độc hại.
- Sử dụng tủ hút: Nếu có thể, nên làm việc trong tủ hút để loại bỏ hơi hóa chất.
6.3. Xử Lý Hóa Chất Cẩn Thận
- Đọc kỹ hướng dẫn sử dụng: Trước khi sử dụng bất kỳ loại oxit bazơ nào, cần đọc kỹ hướng dẫn sử dụng và tuân thủ các quy định an toàn.
- Không trộn lẫn các hóa chất: Tránh trộn lẫn các loại oxit bazơ với nhau hoặc với các hóa chất khác, vì có thể gây ra phản ứng nguy hiểm.
- Sử dụng đúng dụng cụ: Sử dụng các dụng cụ chuyên dụng để lấy và định lượng hóa chất.
6.4. Xử Lý Sự Cố
- Nếu hóa chất dính vào da hoặc mắt: Rửa ngay lập tức bằng nhiều nước sạch trong ít nhất 15 phút và đến cơ sở y tế gần nhất để được xử lý.
- Nếu hít phải hơi hóa chất: Di chuyển đến nơi thoáng khí và đến cơ sở y tế gần nhất để được kiểm tra.
- Nếu hóa chất đổ ra ngoài: Sử dụng các vật liệu thấm hút (như cát, giấy) để thu gom hóa chất và xử lý theo quy định.
6.5. Lưu Trữ Hóa Chất Đúng Cách
- Lưu trữ oxit bazơ trong hộp đựng kín: Để tránh tiếp xúc với không khí và hơi ẩm.
- Để hóa chất ở nơi khô ráo, thoáng mát: Tránh ánh nắng trực tiếp và nhiệt độ cao.
- Để hóa chất xa tầm tay trẻ em: Để đảm bảo an toàn cho trẻ nhỏ.
Tuân thủ các biện pháp an toàn khi làm việc với oxit bazơ là vô cùng quan trọng để bảo vệ sức khỏe và tránh các tai nạn đáng tiếc.
7. Câu Hỏi Thường Gặp (FAQ) Về Oxit Bazơ
Dưới đây là một số câu hỏi thường gặp về oxit bazơ, cùng với câu trả lời ngắn gọn và dễ hiểu:
1. Oxit nào sau đây là oxit bazơ?
Oxit bazơ là hợp chất của kim loại và oxy, ví dụ: Na₂O, CaO, CuO.
2. Oxit bazơ có tan trong nước không?
Một số oxit bazơ tan trong nước (như Na₂O, CaO), một số không tan (như CuO, Fe₂O₃).
3. Oxit bazơ tác dụng với chất gì?
Oxit bazơ tác dụng với axit và một số tác dụng với oxit axit.
4. Oxit bazơ dùng để làm gì?
Oxit bazơ có nhiều ứng dụng, như sản xuất xi măng, khử chua đất, xử lý nước.
5. Làm sao để nhận biết oxit bazơ?
Dựa vào thành phần hóa học, tính chất hóa học và bảng tính tan.
6. Oxit nào sau đây là oxit lưỡng tính?
Al₂O₃ và ZnO là những oxit lưỡng tính phổ biến.
7. Oxit nào sau đây là oxit trung tính?
CO và NO là những oxit trung tính thường gặp.
8. Vôi sống là oxit gì?
Vôi sống là CaO (canxi oxit), một oxit bazơ quan trọng.
9. Tại sao cần phải khử chua đất bằng vôi?
Vôi (CaO) có tính bazơ, giúp trung hòa axit trong đất, cải thiện độ pH, tạo điều kiện cho cây trồng phát triển tốt hơn.
10. Oxit bazơ có độc hại không?
Một số oxit bazơ có thể gây kích ứng da, mắt hoặc hệ hô hấp. Cần tuân thủ các biện pháp an toàn khi sử dụng.
8. CAUHOI2025.EDU.VN – Nguồn Thông Tin Hóa Học Tin Cậy Dành Cho Bạn
Bạn đang gặp khó khăn trong việc tìm kiếm thông tin chính xác và dễ hiểu về hóa học? CAUHOI2025.EDU.VN chính là giải pháp hoàn hảo dành cho bạn!
Tại CAUHOI2025.EDU.VN, bạn sẽ tìm thấy:
- Câu trả lời chi tiết và dễ hiểu: Cho mọi thắc mắc về hóa học, từ cơ bản đến nâng cao.
- Thông tin được kiểm chứng và đáng tin cậy: Từ các nguồn uy tín trong nước.
- Giao diện thân thiện và dễ sử dụng: Giúp bạn dễ dàng tìm kiếm và tiếp cận thông tin.
Đặc biệt, nếu bạn có bất kỳ câu hỏi nào về hóa học, đừng ngần ngại đặt câu hỏi tại CAUHOI2025.EDU.VN. Đội ngũ chuyên gia của chúng tôi luôn sẵn sàng giải đáp và hỗ trợ bạn một cách nhanh chóng và hiệu quả.
Hãy truy cập CAUHOI2025.EDU.VN ngay hôm nay để khám phá thế giới hóa học đầy thú vị và bổ ích!
Địa chỉ: 30 P. Khâm Thiên, Thổ Quan, Đống Đa, Hà Nội, Việt Nam
Số điện thoại: +84 2435162967
Trang web: CAUHOI2025.EDU.VN
Lời kêu gọi hành động (CTA)
Bạn còn thắc mắc nào về oxit bazơ hoặc các hợp chất hóa học khác? Đừng ngần ngại truy cập CauHoi2025.EDU.VN để khám phá thêm nhiều kiến thức hữu ích và đặt câu hỏi của bạn ngay hôm nay! Chúng tôi luôn sẵn sàng hỗ trợ bạn trên hành trình chinh phục môn hóa học.

